
Empresas emergentes que utilizan CRISPR le están dando a la edición del genoma varios giros nuevos. Los editores de bases, las exonucleasas y otras mejoras permiten avances en el reconocimiento de patógenos, el desarrollo de antibacterianos, medicina genética, el xenotrasplante y nuevas aplicaciones agrícolas.
Genetic Engineering & Biotechnology News / 3 de agosto de 2020.- Hace apenas siete años, Feng Zhang, PhD, del Broad Institute, y el genetista George Church, PhD de Harvard, demostraron por separado que en cultivos de células humanas, la edición del genoma se podía realizar utilizando un sistema CRISPR. CRISPR, que en español significa “repeticiones palindrómicas cortas agrupadas regularmente interespaciadas”, salió a la luz por primera vez como parte de un sistema de defensa natural en las bacterias. El ADN-CRISPR en bacterias incluye elementos repetitivos y elementos espaciadores, el último de los cuales codifica moléculas de ARN que forman complejos con una nucleasa asociada a CRISPR (Cas) y la guían hacia objetivos virales, es decir, virus que poseen material genético complementario para guiar el ARN.
Después de que Zhang y Church demostraron que CRISPR-Cas9, uno de los sistemas inmunes adaptativos crudos que se encuentran en las bacterias, tenía potencial como herramienta de ingeniería genómica, muchos desarrolladores siguieron su ejemplo. Las primeras empresas emergentes usando CRISPR, como Editas Medicine, CRISPR Therapeutics e Intellia Therapeutics, se hicieron públicas y desde entonces han prosperado. Y ahora, una nueva cosecha de nuevas empresas está demostrando que todavía hay mucho espacio para la innovación.
Cada una de las nuevas empresas emergentes de CRISPR presenta un giro único respecto a la fórmula original de CRISPR. Los ejemplos de giros en CRISPR incluyen enzimas exóticas y mecanismos de edición novedosos y sofisticados. En este artículo se presentan cinco startups que usan CRISPR. Sus aplicaciones van desde hacer que las verduras tengan mejor sabor hasta diagnosticar COVID-19 en entornos de bajos recursos.
Fabricación de órganos seguros para trasplantes
La inactivación de un virus es una extensión lógica de la función natural del sistema CRISPR-Cas9, y ofrece una solución única para un viejo problema: la escasez de órganos y tejidos humanos para trasplante. El xenotrasplante de órganos de cerdos a humanos se ha contemplado durante más de un siglo. Los órganos de los cerdos son comparables a los órganos humanos en tamaño y función, y los cerdos se pueden criar en cantidades lo suficientemente grandes como para satisfacer la necesidad de órganos. Pero el progreso en los xenotrasplantes se detuvo en la década de 1990 debido a la presencia de retrovirus endógenos porcinos (PERV) en el genoma del cerdo.
En 2017, un grupo liderado por George Church y Luhan Yang inactivó con éxito todos los PERV en una célula primaria porcina y creó cerdos con PERV inactivados mediante transferencia nuclear de células somáticas (clonación). La pareja fundó una nueva empresa, eGenesis, que se dedica al desarrollo de órganos, tejidos y células trasplantables seguras mediante el uso de la edición de genes con CRISPR para inactivar los PERV.
William Westlin, PhD, vicepresidente ejecutivo de investigación y desarrollo de eGenesis, dice que la compañía ha producido más de 350 cerdos modificados genéticamente, algunos de los cuales ahora tienen un par de años. “Hacemos entre decenas y cientos de modificaciones en el genoma eliminando genes porcinos, insertando genes humanos y humanizando genes porcinos”, detalla. “Es un enfoque multiplé. El producto clínico combinará modificaciones inmunológicas sobre un fondo de retrovirus endógeno inactivado “.
Westlin estima que dentro de un par de años, eGenesis comenzará estudios clínicos sobre sus programas de células de islotes pancreáticos y de riñón principal. La compañía planea expandir su oferta de productos a aplicaciones como el xenotrasplante de corazón, hígado, córnea, retina y células neurales.
Las enzimas extremófilas ofrecen una nueva funcionalidad
Aunque CRISPR-Cas9 es el sistema CRISPR más conocido y más utilizado, existen otros sistemas CRISPR en la naturaleza, sistemas que están siendo perseguidos por Caspr Biotech, una empresa que está desarrollando diagnósticos basados en nuevas enzimas CRISPR descubiertas en entornos extremos en todo el mundo. El cofundador y CEO de Caspr, Franco Goytia, dice que la compañía ha organizado expediciones por Sudamérica y la Antártida en busca de entornos hostiles (como desiertos, regiones de gran altitud y entornos con alta salinidad y alta radiación UV) para organismos con nuevos sistemas CRISPR. La cartera de enzimas de la empresa incluye funcionalidades únicas que normalmente se correlacionan con los entornos originales de las enzimas.
Como ejemplo de esa funcionalidad, Goytia dice que muchos sistemas CRISPR operan a temperaturas de alrededor de 37 °C. Sin embargo, esas temperaturas no son compatibles con la amplificación isotérmica, que funciona mejor a 62–64 °C. “Tener cualquier cosa que pueda tolerar esa temperatura más alta”, señala Goytia, “es algo muy estratégico para la amplificación”.
El inicio de la pandemia de COVID-19 presentó desafíos importantes, pero también una gran oportunidad, ya que Caspr tenía las herramientas para desarrollar rápidamente un kit de diagnóstico para la detección del ARN del SARS-CoV2. “Nuestro equipo estaba formado básicamente por seis o siete personas”, recuerda Goytia. “Cuando surgió COVID-19, sabíamos que se trataba de una aplicación perfecta y que habría una necesidad generalizada de más kits que tuvieran un componente de accesibilidad adicional”.
[Recomendado: Esfuerzos de tratamiento para COVID-19 utilizando plantas e ingeniería genética]Caspr estableció un marco de tiempo de desarrollo agresivo para construir un kit prototipo y luego producir e implementar a escala. En tres meses, la empresa había presentado una solicitud de autorización de uso de emergencia a la FDA. El kit combina un paso de transcripción inversa, amplificación isotérmica y una enzima CRISPR-Cas para detección de objetivos en un kit portátil, accesible en un entorno de baja complejidad o bajos recursos, y capaz de completar análisis en menos de 60 minutos. El kit no requiere equipos o reactivos de reacción en cadena de la polimerasa cuantitativa (qPCR), solo un lector de placas de fluorescencia y un equipo de laboratorio simple, como un bloque de calor y micropipetas.
Goytia indica que en lugar de centrarse en un objetivo específico, la empresa está desarrollando una plataforma. Los programas en trámite incluyen los que abordan el dengue, el virus zika, el hantavirus y las superbacterias resistentes a los antibióticos. Caspr también planea expandirse a industrias fuera de la atención médica, como la agricultura.
Reescribiendo genes para reducir el colesterol
Verve Therapeutics fue fundada en 2018 por Sekar Kathiresan, MD, y otros investigadores en el área de la genética cardiovascular, incluidos Kiran Musunuru, MD, PhD y J. Keith Joung, MD, PhD. Una inversión inicial de $58,5 millones de dólares permitió a la empresa obtener la licencia de la tecnología de edición de base de Beam Therapeutics y la tecnología CRISPR de la Universidad de Harvard y el Broad Institute.
Como profesor de medicina en la Escuela de Medicina de Harvard, Kathiresan dirigió un esfuerzo de investigación que descubrió ocho genes que albergan lo que él llama mutaciones de resistencia. “Como resultado de la mutación, el gen se apaga”, dice Kathiresan. Agrega que las personas que portan la mutación tienen el colesterol bajo durante toda la vida y están “extraordinariamente protegidas contra un ataque cardíaco”.
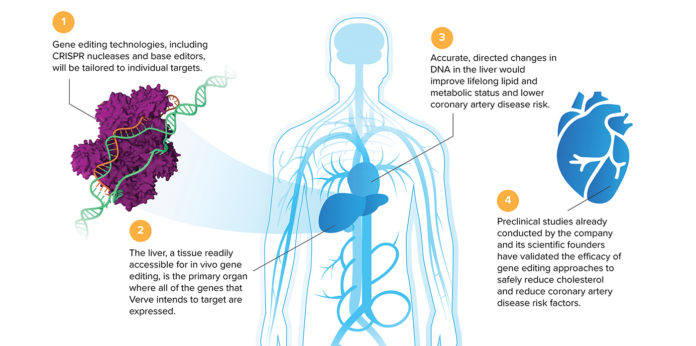
El enfoque de Verve se basa en esos ocho genes que albergan mutaciones de resistencia. El producto principal de la empresa consiste en una nanopartícula lipídica que encierra ARNm CRISPR y un ARN guía. Está diseñado para desactivar el gen diana en la célula del hígado.
En la edición estándar de CRISPR-Cas9, la enzima corta ambas cadenas de ADN y luego los mecanismos innatos de reparación del ADN de la célula introducen cambios de secuencia en esos sitios objetivo. Con la edición de base, un Cas9 que ha tenido su capacidad de corte deshabilitada se empareja con una segunda enzima que cambia una sola base de una letra a otra, de adenina (A) a guanina (G), por ejemplo.
El método de edición básico ofrece precisión adicional. Sin embargo, tanto el CRISPR-Cas9 estándar como la edición de bases pueden generar efectos fuera de objetivo. Esos efectos fuera del objetivo presentan un problema potencial que Verve está monitoreando en sus estudios. “Es un desafío clave”, enfatiza Kathiresan, “encontrar la combinación correcta de ARNm del editor y ARN guía que le brindará la máxima edición en el objetivo y una mínima o ninguna edición fuera del objetivo”.
Hasta ahora, el diseño de la empresa funciona. Después de obtener resultados positivos en modelos de ratón, Verve informó recientemente los resultados de un estudio de prueba de concepto en 14 primates no humanos que muestran una reducción del 59% en los niveles de colesterol LDL en sangre para un programa dirigido a PCSK9. Para otro programa dirigido a ANGPTL3, los triglicéridos en sangre se redujeron en un 64% y el colesterol LDL se redujo en un 19%. Además, en los hepatocitos humanos primarios, no hubo evidencia de edición fuera del objetivo. Verve espera avanzar a los primeros estudios en humanos dentro de tres años.
CRISPR para frutas y verduras
Pairwise es otra empresa con tecnología licenciada por Harvard y el Broad Institute, además del Massachusetts General Hospital. A diferencia de Verve, Pairwise ha ido en la dirección de la agricultura, utilizando la edición de genes con CRISPR para hacer que las frutas y verduras saludables sean más sabrosas. Tom Adams, PhD, es el director ejecutivo de Pairwise y cofundador de Haven Baker, PhD.
[Recomendado: Start-Up desarrolla frutas y verduras más sabrosas utilizando edición genética con CRISPR]La empresa recibió financiación inicial de Monsanto (ahora Bayer) y Deerfield Capital. Además de colaborar con Bayer en proyectos tradicionales de maíz y soya, Pairwise está delimitando su propio territorio en frutas y verduras. “Nuestro punto de vista era que no ha habido tanta innovación y tanta tecnología en los productos como en el maíz y la soja”, relata Adams. “Se refleja en el hecho de que las personas no comen las verduras que se supone que deben comer. Pensamos que había una oportunidad real con la edición de genes para crear algunas características novedosas basadas en el consumidor en los productos “.
[Recomendado: Desarrollarán nuevas variedades de berries usando edición genética con CRISPR]Específicamente, Pairwise está desarrollando productos en verduras de hoja verde. Su primer producto de hojas verdes será una forma de hojas de mostaza que carece del sabor fuerte caractetístico de la mostaza convencional. A diferencia de la col rizada y otras verduras con alto contenido de nutrientes que tienen rendimientos relativamente bajos en comparación con lechugas menos nutritivas como la lechuga romana y iceberg, las nuevas hojas de mostaza tienen un alto contenido de nutrientes y un alto rendimiento. Pairwise también está desarrollando moras sin semillas y cerezas sin cuesco mientras explora formas adicionales de llevar nuevas variedades al mercado.
Además de iniciar sus programas de desarrollo de productos, Pairwise ha secuenciado 700 variedades de berries como parte de un consorcio público-privado. “El 99% de los rasgos en las bayas son causados por cambios en la secuencia codificante del gen, más que fuera de la secuencia codificante”, señala Adams. “Nuestra tecnología está muy bien adaptada para ofrecer las cosas que queremos hacer porque podemos editar eficazmente dentro de las secuencias de genes”.
Nuevos antibacterianos
Mientras que CRISPR-Cas9 es bien conocida como una herramienta para la edición de genes, están surgiendo otras enzimas CRISPR con diferentes funciones y aplicaciones más allá de la edición de genes. Locus Biosciences está desarrollando productos antibacterianos basados en CRISPR-Cas3 para buscar indicaciones contra patógenos bacterianos convencionales y aplicaciones de microbiomas.
Uno de los productos de la empresa se llama CRISPR-phage o crPhage. Este producto utiliza bacteriófagos diseñados que infectan específicamente a las bacterias y se mejoran mediante el uso de un sistema CRISPR-Cas3 único para atacar el genoma bacteriano.
[Recomendado: Edición genética para luchar contra las ‘súper bacterias’ resistentes a antibióticos]“Cas3 es una exonucleasa”, dice Joseph Nixon, vicepresidente senior de desarrollo comercial de Locus. “Es diferente de otros sistemas CRISPR porque abre, desenrolla y tritura el ADN genómico específico en las células bacterianas, matando así esas células porque no pueden reparar el daño extenso de Cas3”.
Locus fue fundado por Paul Garofolo y Dave Ousterout, PhD, en 2015 con tecnologías Cas3 con licencia de la Universidad Estatal de Carolina del Norte y la Universidad de Duke. La compañía está avanzando rápidamente hacia la parte clínica, con su producto antibacteriano líder actualmente en pruebas clínicas de fase I para el tratamiento de infecciones del tracto urinario causadas por Escherichia coli.
“Nuestro ensayo en curso es uno de los primeros estudios clínicos bien controlados para la terapia con fagos”, afirma Paul Kim, PhD, director de desarrollo de Locus. “Representa un paso emocionante para ayudar a los pacientes que padecen infecciones recurrentes y resistentes a múltiples fármacos”.

