CRISPR
CRISPR es una técnica de edición génica que permite cortar el ADN en un sitio específico para después editarlo. CRISPR (del inglés: Clustered Regularly Interspaced Short Palindromic Repeats, en español repeticiones palindrómicas cortas agrupadas y regularmente interespaciadas) son familias de secuencias de ADN bacterianas que contienen fragmentos de ADN de virus que han atacado a las bacterias. Estos fragmentos son utilizados por la bacteria para detectar y destruir el ADN de nuevos ataques de virus similares, y así poder defenderse eficazmente de ellos.
Los CRISPR contienen repeticiones cortas de secuencias de bases y tras cada repetición siguen segmentos cortos de “ADN espaciador” proveniente de distintos virus que han atacado previamente a la bacteria.
Este sistema se encuentra en aproximadamente el 40% de los genomas bacterianos y en el 90% de los genomas secuenciados de las arqueas. Con frecuencia se hallan asociados con los genes cas, que codifican para proteínas nucleasas relacionadas con los CRISPR. El sistema CRISPR/Cas es un sistema inmunitario procariótico que confiere resistencia a agentes externos como plásmidos y fagos (virus bacterianos) y provee una forma de inmunidad adquirida. Así, cuando un virus infecta una bacteria, su ADN se fragmenta y se incluye en el genoma del microorganismo, para después transcribir pequeños ARNs que actuarán como guías de las nucleasas Cas, para que reconozca y destruya el ADN del virus en posteriores infecciones.
Funcionamiento
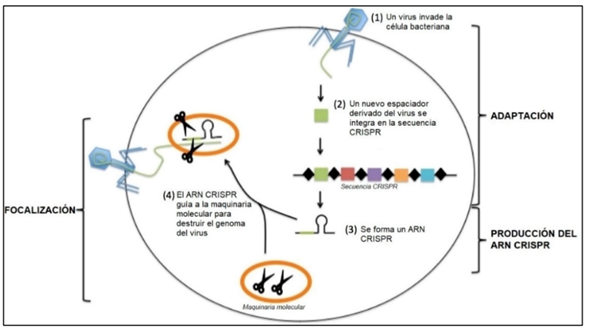
El funcionamiento del sistema inmune CRISPR se puede resumir en tres procesos fundamentales:
1) Proceso de adaptación: cuando un ADN de un virus que ha infectado la bacteria es cortado en segmentos pequeños que son insertados en la secuencia CRISPR como nuevos espaciadores.
2) Proceso de producción de ARN-CRISPR: las repeticiones CRISPR y los espaciadores que se encuentran en el ADN de la bacteria pasan por un proceso de transcripción. El ARN resultante se corta en fragmentos que reciben el nombre de ARNs-CRISPR.
3) Proceso de focalización (o targeting): los ARNs-CRISPR guían a la maquinaria molecular para destruir el material viral. Pueden actuar como guías ya que las secuencias de ARN-CRISPR han sido copiadas de un ADN viral y son complementarias de los fragmentos del genoma viral.
Figura 1. Pasos de la inmunidad mediada por el sistema CRISPR. Las regiones CRISPR están compuestas por repeticiones de ADN pequeño (representadas por los rombos negros) y espaciadores (representados por cuadrados de colores). Figura tomada de Fundación Antama.
Descubrimiento
En 1987 se publicó un artículo en el cual se describía cómo algunas bacterias (Streptococcus pyogenes) se defendían de los virus. Estas bacterias tienen unas enzimas que son capaces de distinguir entre el material genético de la bacteria y el del virus y, una vez hecha la distinción, destruyen al material genético del virus.
Con el tiempo, se encontró que una zona determinada del genoma de muchos microorganismos, sobre todo arqueas, estaba llena de repeticiones palindrómicas (que se leen igual al derecho y al revés) sin ninguna función aparente. Estas repeticiones estaban separadas entre sí mediante unas secuencias denominadas “espaciadores” que se parecían a otras de virus y plásmidos. Justo delante de esas repeticiones y “espaciadores” hay una secuencia llamada “líder”. Estas secuencias son las que se llamaron CRISPR (“Repeticiones Palindrómicas Cortas Agrupadas y Regularmente interespaciadas”). Muy cerca de este agrupamiento se podían encontrar unos genes que codificaban para un tipo de nucleasas: los genes cas.
Durante años subsiguientes se continuó la investigación sobre este sistema, pero no fue hasta el año 2012 en el que se convirtió este sistema inmune de las bacterias en una herramienta molecular útil en el laboratorio. Un equipo de investigadores dirigido por las doctoras Emmanuelle Charpentier en la Universidad de Umeå y Jennifer Doudna, en la Universidad de California en Berkeley, demostraron cómo convertir esa maquinaria natural en una herramienta de edición “programable”, que servía para cortar cualquier cadena de ADN in vitro. Es decir, lograron programar el sistema para que se dirigiera a una posición específica de un ADN cualquiera (no solo vírico) y lo cortaran.
Sistema CRISPR/Cas
CRISPR-Cas es el nombre que recibe el sistema formado por CRISPR y las proteínas asociadas Cas (en inglés, CRISPR-associated) que confiere inmunidad adaptativa contra elementos exógenos como virus en muchas bacterias y la mayor parte de las arqueas. Las proteínas Cas son nucleasas, es decir, cortan el ADN de forma específica guiadas por secuencias de ARN.
Los sistemas CRISPR-Cas son muy diversos, ya que cada bacteria y cada arquea tiene el suyo propio. Por ello, se ha creado una clasificación en la que los sistemas se dividen en dos clases, que a su vez contienen diferentes tipos, que se diferencian según las características específicas de las nucleasas. Destacan los sistemas que pertenecen a la clase II , ya que han sido modificados por ingeniería genética para actuar de forma más robusta, con el fin de realizar modificaciones más eficaces en el genoma de múltiples sistemas eucariotas, como por ejemplo las células humanas.
CRISPR-Cas9 es uno de los sistemas que se encuentra dentro de los de clase II, y deriva de una bacteria llamada Streptococcus pyogenes. Este sistema que ha sido adaptado para la edición de genomas está compuesto por la proteína Cas9 (nucleasa asociada a CRISPR) y un sgARN (single-guided RNA) que actúa como ARN guía dirigiendo a Cas9 al sitio diana. Este sgARN está compuesto por tan solo 20 nucleótidos. La nucleasa y el ARN guía o sgARN funcionan asociados formando un complejo.
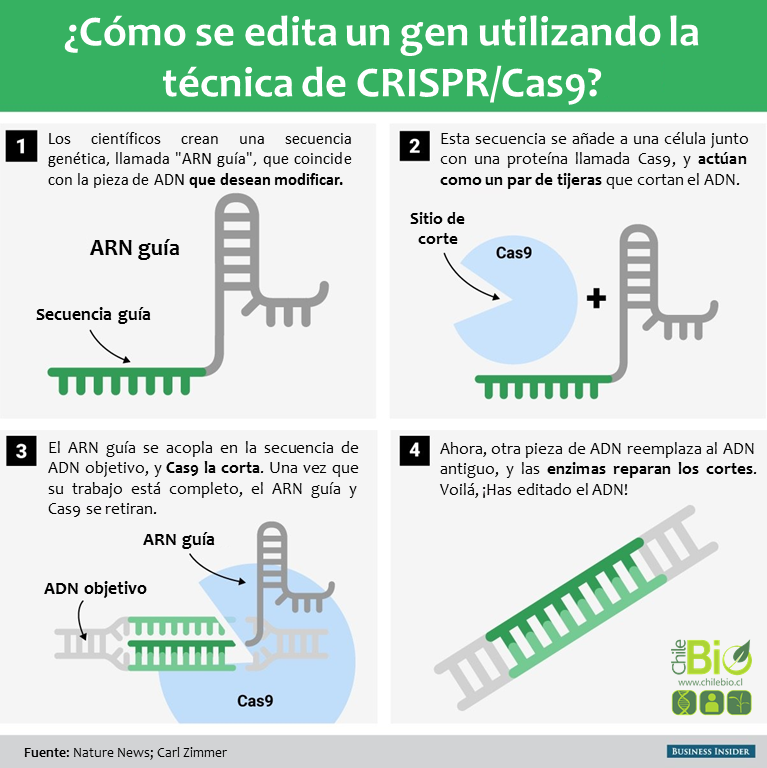
Editando el ADN con esta tecnología
Todo comienza con el diseño de una molécula de ARN (CRISPR o ARN guía) que luego va a ser insertada en una célula. Una vez dentro reconoce el sitio exacto del genoma donde la enzima Cas9 deberá cortar.
En una primera etapa, el ARN guía se asocia con la enzima Cas9. Este ARN guía es específico de una secuencia concreta del ADN, de tal manera que por las reglas de complementariedad de nucleótidos se hibridará en esa secuencia (la que nos interesa editar o corregir). Entonces actúa Cas9, que es una enzima endonucleasa (es decir, una proteína que es capaz de romper un enlace en la cadena de los ácidos nucléicos), cortando el ADN.
En una segunda etapa se activan al menos dos mecanismos naturales de reparación del ADN cortado. El primero llamado indel (inserción-deleción) hace que, después del sitio de corte (la secuencia específica del ADN donde se unió el ARN guía), bien aparezca un hueco en la cadena, bien se inserte un trocito más de cadena. Esto conlleva a la perdida de la función original del segmento de ADN cortado.
Un segundo mecanismo permite la incorporación de una secuencia concreta exactamente en el sitio original de corte. Para esto, lógicamente, hemos de darle a la célula la secuencia que queremos que se integre en el ADN.
Uso de CRISPR en vegetales
Con el sistema CRISPR se están llevando a cabo modificaciones dirigidas en el genoma de especies de interés agronómico en las que las técnicas de manipulación o mejora genética convencionales eran costosas o incluso inviables.
Con CRISPR se producen resultados idénticos a los que se producirían con los métodos convencionales de mejoramiento genético vegetal, pero de forma más predecible, rápida y barata. La mayoría de las aplicaciones apuntan a mejorar caracteres como el rendimiento, la arquitectura de la planta y la tolerancia a enfermedades.
Tanto CRISPR-Cas9 como CRISPR-Cpf1 (sistema CRISPR procedente de la bacteria Francisella tularensis) son los dos sistemas mejor estudiados y más usados en plantas, pero se están investigando nuevas versiones.
Algunos de los usos prometedores en agricultura se han mostrado en cultivos de trigo, maíz y tomate, desarrollando variedades mejoradas en caracteres como la defensa frente a plagas, la adaptación a la sequía, el rendimiento, y también la calidad y las características nutricionales para el consumidor. Algunos ejemplos de estos usos que se han llevado a cabo con éxito son el trigo sin gluten apto para celiacos, plantas de tomate resistentes a las altas temperaturas gracias a la inactivación de un solo gen y maíz resistente a la sequía.
Otros ejemplos de aplicaciones más concretos han sido llevados a cabo en arroz y soja. En el caso del arroz, CRISPR ha sido usado para obtener panículas más densas y erectas, y plantas de menor altura, lo que conlleva un mayor rendimiento.